В этом разделе опубликована информация в о вакцинах против Covid-19 в Европейском союзе.
21 декабря 2020 года Европейское агентство лекарственных средств (ЕАЛС) рекомендовало выдать условное разрешение на регистрацию вакцины Comirnaty, разработанной BioNTech и Pfizer, и Европейская комиссия одобрила (зарегистрировала) эту вакцину для использования на всей территории Европейского союза. Она предназначена для предотвращения инфицирования коронавирусом (Covid-19) людей в возрасте от 5 лет.
6 января 2021 года ЕАЛС рекомендовало провести условную регистрацию вакцины от Covid-19 Moderna (Spikevax), которая также была одобрена Европейской комиссией для использования в ЕС. Она предназначена для предотвращения инфицирования коронавирусом (Covid-19) людей в возрасте от 6 лет. Это вторая вакцина против Covid-19, одобренная для использования в ЕС.
29 января 2021 года Европейское агентство лекарственных средств (ЕАЛС) рекомендовало зарегистрировать в Европейском союзе вакцину Covid-19 Vaccine AstraZeneca "Vaxzevria" c условием. Эта вакцина предназначена для предотвращения заболевания Covid-19 у людей старше 18 лет. Чтобы вакцина была зарегистрирована для использования во всех странах-членах Европейского союза, еще необходимо получить разрешение Европейской комиссии. Согласно предоставленной производителем информации первая поставка этих вакцин Национальной службе здоровья (НСЗ) планируется в феврале этого года.
11 марта 2021 года Европейское агентство лекарств рекомендовало в Европейском союзе (ЕС) зарегистрировать с условиями вакцину ''Jcovden'' (Janssen). Эта вакцина предназначена для предотвращения инфекции коронвируса для людей с 18 лет.
20 ноябрь 2021 года Европейское агентство лекарств рекомендовало в Европейском союзе (ЕС) зарегистрировать с условиями вакцину «Nuvaxovid» (Novavax).
23 июня 2022 года Европейское агентство лекарств рекомендовало в Европейском союзе (ЕС) зарегистрировать Valneva вакцину “COVID-19 Vaccine (inactivated, adjuvanted) Valneva”.
Комитет ЕАЛС по лекарственным препаратам для человека (КЛПЧ) произвел строгую оценку качества, безопасности и эффективности обеих вакцин и принял однозначное решение рекомендовать выдать формальное свидетельство об условной регистрации. Свидетельства выдала Европейская комиссия. Это гарантирует получение жителями Европейского союза вакцины, соответствующей требованиям ЕС, а также соблюдение мер безопасности, осуществление контроля и обеспечение условий для проведения кампаний вакцинации в масштабах Европейского союза.
В настоящее время в процессe ускоренной регистрации Европейское агентство лекарств (EZA) оценивает заявление "Sputnik V", "Sinovac", Sanofi Pasteur вакцина "Vidprevtyn".
Информация от Государственного агентства лекарств о разработке, научном исследовании, наблюдении за вакциной, а также важная информация о вакцинах:
Не становись жертвой мифов о вакцинации против Covid-19! Государственное агентство лекарств предоставляет информацию, основанную на доказательствах
На сегодняшний день в Латвии зарегистрировано три вакцины против Covid-19, но более 200 вакцин все еще находятся в стадии разработки. Как стало возможным менее чем за год разработать вакцины, достаточно безопасные и эффективные для использования? Государственное агентство лекарств (ZVA) предоставляет информацию, основанную на научных доказательствах, чтобы развеять 12 самых распространенных мифов относительно безопасности, составе и эффективности зарегистрированных вакцин против Covid-19.
# 1 Вакцину невозможно разработать в течение года
Возможно это покажется невероятным, но в наши дни, благодаря прогрессу науки, высоким достижениям в области разработки вакцин, технологическим решениям, эффективному сотрудничеству и оперативным действиям ученых, производителей и регистрирующих учреждений, это произошло! Как? Исследователи уже более 10 лет изучали вирусы SARS и MERS и работали над созданием вакцин против этих вирусов, что и стало основой быстрой разработки вакцин против Covid-19. Причем для разработки этих вакцин были использованы научные, финансовые и человеческие ресурсы, не имеющие аналога в истории. В процессе разработки и анализа вакцин участвовало огромное количество экспертов и ученых, которые проводили качественное тестирование вакцин в соответствии с неизменно строгими требованиями к их регистрации.
# 2 Вакцины небезопасны и вызывают опасные для жизни побочные эффекты
Не существует лекарств или вакцин, не имеющих побочных эффектов. Любое лекарство утверждается, то есть регистрируется только в том случае, если получены надежные данные, свидетельствующие, что их преимущества превосходят риски. Это касается и вакцин, которые утверждаются, только если их преимущества многократно превышают риски. Как и все лекарства, вакцины против Covid-19 были тщательно протестированы в соответствии c высокими требованиями o безопасности, качестве и эффективности. Никаких отступлений от строгих требований ни при разработке, ни при регистрации допущено не было.
Как после приема любого лекарства, так и после вакцинации против Covid-19 в некоторых случаях могут возникать кратковременные реакции организма, вызванные процессами формирования иммунитета. Наиболее распространенными реакциями являются, например, повышенная температура, лихорадка, головная боль, чувство усталости, боль или покраснение в месте инъекции.
Обычно эти реакции наиболее явно выражены после введения второй дозы вакцины Pfizer-BioTech и Moderna (Spikevax) и после первой дозы вакцины AstraZeneca. Реакции обычно возникают в первые дни после вакцинации, длятся несколько дней и затем исчезают.
В случае, если после вакцинации против Covid-19 появились какие-либо побочные эффекты, вызывающие у вас опасения, если вы чувствуете кратковременное снижение работоспособности, сообщите об этом врачу. Врач, фармацевт, а также пациент могут сообщать о констатированных побочных эффектах, вызванных лекарством, в частности вакциной, в Государственное агентство лекарств, на веб-сайте www.zva.gov.lv > "Ziņot par zāļu blaknēm, negadījumiem ar ierīcēm un biovigilanci".
Важное значение имеет и тщательный последующий контроль за действием вакцин. В соответствии с планом мониторинга безопасности вакцин против Covid-19 латвийское и другие агентства лекарств ЕС постоянно собирают и анализируют новейшую информацию о вакцинах против Covid-19 и других лекарствах в целях обеспечения безопасности вакцин и лекарств и охраны здоровья населения.
# 3 Третья фаза клинических исследований воздействия вакцин на людей не проводилась
Регистрация вакцин или лекарств невозможна без выполнения одного из основных требований для регистрации – представления результатов третьей фазы клинических исследований воздействия на людей и их анализа Европейским агентством лекарств. Зарегистрированные вакцины против Covid-19 прошли эту фазу испытаний, полученные результаты были проанализированы и одобрены Европейским агентством лекарств.
В клинических испытаниях приняли участие десятки тысяч человек. В клинических испытаниях вакцины Comirnaty, разработанной Pfizer-BionTech, участвовало в целом около 44 000 человек. В клинических испытаниях вакцины Moderna (Spikevax) приняли участие примерно 30 000 человек. Около 24 000 человек участвовало в клинических испытаниях вакцины Vaxzevria.
# 4 Качество вакцины зависит от производителя
Все зарегистрированные в Латвии вакцины очень эффективны в предотвращении тяжелого заболевания, вызванного Covid-19. Ни одна из утвержденных вакцин не может считаться лучшей или худшей. Все зарегистрированные вакцины одинаково тщательно протестированы, одинаково качественны, эффективны и безопасны. Вакцины регистрируются только в том случае, если Европейское агентство лекарств получает доказательства того, что преимущества вакцин намного превосходят риски. Кроме того, для подтверждения качества вакцин проводится их сравнительное исследование.
# 5 Вакцины не защищают от новых типов вируса Covid-19
Доказано, что зарегистрированные на сегодняшний день вакцины против Covid-19 защищают также от новых разновидностей вируса. Но с учетом того, что некоторые из новых типов вируса все же могут снизить способность вакцин защищать от инфекции и развития заболеваний, Европейское агентство лекарств попросило производителей вакцин предoставить дополнительные доказательства эффективности препаратов.
# 6 Неизвестно, как долго вакцина будет защищать от Covid-19
Исследования показывают, что все утвержденные на сегодняшний день вакцины обеспечивают защиту от Covid-19 в течение не менее 2 месяцев. Вакцина предотвращает симптоматическое заболевание, в частности тяжелое течение болезни и смерть.
Исследования относительно продолжительности действия вакцин продолжаются. Разработчики вакцин проводят также наблюдения за вакцинированными участниками долгосрочных исследований с целью определения точной продолжительности действия вакцин.
# 7 Вакцины не защитят, так как ни одна из них не доказала свою 100-процентную эффективность
Вакцины облегчают течение болезни и предотвращают тяжесть заболевания, вызывая при воздействии вируса защитную реакцию иммунной системы. Исследования продемонстрировали эффективность вакцин в предотвращении симптоматических заболеваний, в частности тяжелого течения болезни.
До утверждения вакцины проводились исследования, участники которых были разделены на
две группы. Одной группе была введена вакцина, другой – плацебо (имитация вакцины). Анализировалось количество заболевших участников обеих групп и на основании результатов рассчитывалась эффективность вакцины. Изучение некоторых вакцин продолжаются. Результаты долгосрочных исследований позволят получить дополнительные данные об эффективности и продолжительности действия вакцин.
# 8 Вакцина не действует на людей в возрасте от 65 лет
Всемирная организация здравоохранения, Европейское агентство лекарств и Латвийский государственный совет по иммунизации, проанализировав имеющиеся данные, подтвердили, что вакцина, разработанная Vaxzevria, обеспечивает защиту от Covid-19 людей всех возрастных групп – от 18-летних до пожилых.
Научные эксперты Европейского агентства лекарств, проведя тщательный анализ вакцины Vaxzevria и порекомендовав зарегистрировать ее в Европе, отметили, что упомянутая вакцина обеспечит защиту также пожилых людей.
На основании опыта использования других вакцин и с учетом того, что после введения вакцины Vaxzevria иммунный ответ наблюдался также у пожилых людей, можно утверждать, что вакцина способна защитить от вируса и людей старшего поколения, несмотря на то, что пока нет достаточных статистических данных, позволяющих сделать вывод о степени защитного воздействия вакцины на людей старше 65 лет.
При этом есть убедительные доказательства безопасности вакцин для этой возрастной группы.
# 9 Вакцины вредны для женщин, планирующих беременность, беременных или кормящих грудью
Основываясь на результатах тщательного анализа вакцин, врачи подтверждают, что вакцины не причиняют вреда беременным, планирующим беременность или женщинам, кормящим грудью. Вакцины не причиняют вреда ни беременным женщинам, ни будущему ребенку, ни новорожденному. Это подтверждается как новейшими лабораторными исследованиями, так и результатами проводимой во всем мире вакцинации миллионов людей, позволяющими судить о долгосрочном воздействии вакцин.
Вакцинация настоятельно рекомендуется врачами женщинам, входящим в группы риска, поскольку преимущества вакцины превосходят риски. Тем не менее беременная женщина, прежде чем пройти вакцинацию, должна проконсультироваться с врачом, так как только врач может дать рекомендацию относительно вакцинации, учтя преимущества и риски для женщины и ребенка.
# 10 Вакцины содержат эмбриональные клетки и микрочипы
Вакцины были созданы искусственным путем, в лабораториях, поэтому не содержат живых вирусов. При производстве вакцин не использовались клетки человека, эмбрионов, животных или микрочипы.
# 11 Вакцины могут быть использованы для детей
Нет, созданные вакцины не предназначены для вакцинации детей младше 16 лет. Вакцину, разработанную Pfizer-BioNTech, можно использовать для вакцинации лиц в возрасте с 16 лет, вакцины, разработанные Moderna (Spikevax) и Vaxzevria, предназначены для вакцинации лиц в возрасте с 18 лет. Производители начали клинические испытания, чтобы проверить пригодность вакцины против Covid-19 для детей.
# 12 Достоверная информация о вакцинах не доступна
Для предоставления жителям достоверной и научно-обоснованной информации о вакцине против Covid-19 на веб-сайте ZVA www.zva.gov.lv в разделе “Covid-19 ziņas” регулярно публикуется и обновляется информация о разработке, анализе, эффективности, качестве и безопасности и утверждении вакцин, а также факты о вакцинах (fakti par vakcīnām).
Информация о порядке вакцинации в Латвии публикуется на веб-сайте Центра профилактики и контроля заболеваний в разделе "Vakcīnas pret Covid-19". Подать заявку на вакцинацию против Covid-19 жители Латвии могут на веб-сайте www.manavakcina.lv. Вакцинация против Covid-19 является добровольной и полностью финансируется государством.
Факты о вакцинах против Covid - 19: pазработка вакцины продолжается
Почему срочно необходимы вакцины против Covid-19?
- Цель вакцин против Covid-19 – защитить людей от болезни, которую вызывает новый коронавирус SARS-CoV-2, содействуя появлению защитной реакции организма.
- Проходящая в настоящее время пандемия вызываемой коронавирусом болезни Covid-19 является кризисом мирового масштаба, который оказывает разрушительное воздействие на здоровье человека, социальные процессы и экономику.
- Covid-19 может привести к тяжёлому заболеванию и даже к смерти у людей всех возрастов, в том числе и у тех, кто не имеет других болезней. К тому же, в настоящий момент мало изучены долгосрочные последствия этого заболевания на здоровье человека.
- Надёжные и эффективные вакцины против Covid-19 необходимы затем, чтобы защитить от заболевания коронавирусной болезнью каждого человека, и в особенности медицинских работников и самые незащищённые группы жителей, а именно пожилых людей и людей с хроническими заболеваниями.
Какие действия и методы в настоящий момент используются, чтобы разработать и утвердить вакцины против Covid-19?
- Вакцины против Covid-19 разрабатываются с учётом тех же самых, строгих требований к качеству, безопасности и качеству, как и в отношении любых других лекарств.
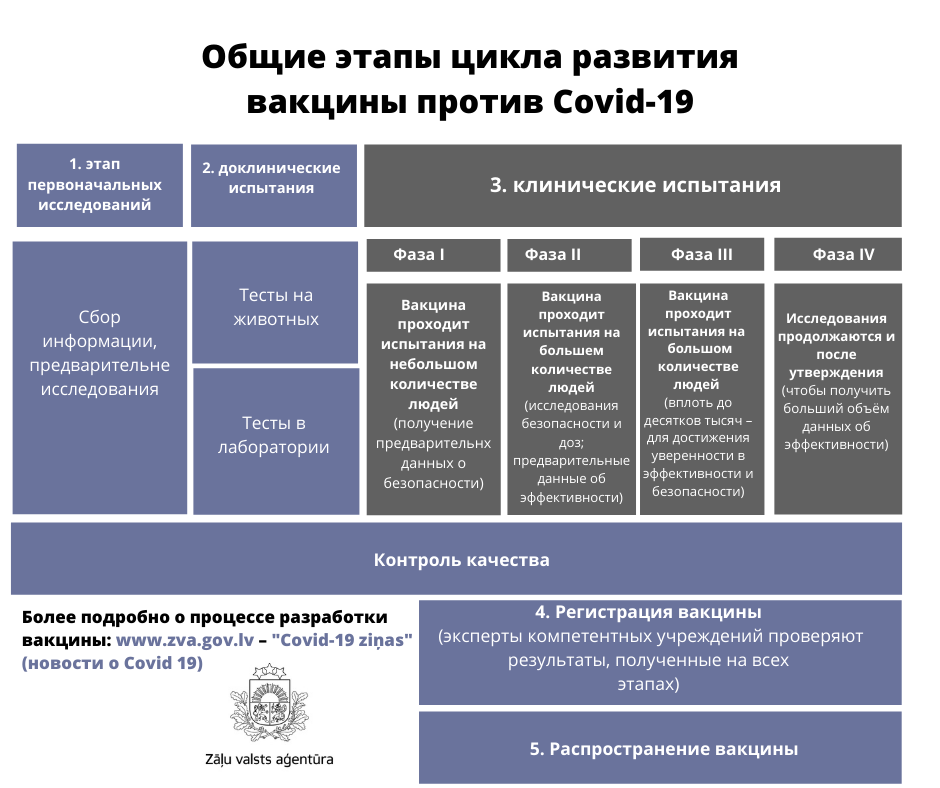
Общие этапы цикла развития вакцины
Этап первоначальных исследований
- Доклинические исследования, в рамках которых эффективность и безопасность вакцины проверяется на животных
- Клинические исследования
- Оценка и утверждение (или регистрация) регулятором
- После регистрации осуществляется надзор, в рамках которого ведётся контроль побочных действий и эффективности в долгосрочной перспективе в рамках всего общества и всех пациентов, которые применяли вакцину.
Клинические исследования состоят из трёх этапов, или фаз. В I фазе вакцину получает совсем небольшое количество людей. Во II фазе клинические исследования расширяются, и вакцину получают люди, имеющие определённые индикации (например, возраст и состояние здоровья), которые похожи на тех людей, которым новая вакцина предназначена. Во время III фазы вакцину вводят десяткам тысяч человек ,а также проверяют её эффективность и продолжают вести надзор за безопасностью в уже намного более широком масштабе. Последним этапом клинических испытаний является IV фаза, и для многих вакцин исследования IV фазы продолжаются и после того, как вакцина была утверждена. Это означает, что эффективность всех лекарств, также и вакцины против Covid-19 первоначально проверяется в лаборатории, в том числе сначала на животных, и только потом к клиническим испытаниям подключаются добровольцы. В обычно ситуации эти этапы осуществляются последовательно, один за другим, чтобы уменьшить возможность того, что неперспективный продукт развивали бы в ходе всех фаз. Чтобы ускорить разработку вакцины Covid-19, определённая часть необходимых этапов осуществляется параллельно. В процессе разработки новой вакцины применяются как уже известные методы, продолжительное время использующиеся при разработке вакцин, так и инновационные методы. Исследователи уже на протяжении более 10 лет изучали потенциальные вакцины против вирусов SARS и MERS. Эти, продолжающиеся длительное время исследования заранее послужили основой для более быстрой разработки препаратов, которые могут быть кандидатами на статус вакцины в ходе этой пандемии.
Дополнительная информация
В настоящий момент разработка вакцин против Covid-19 опирается на различные технологии производства вакцин, предназначенных для человека. Часть из них хорошо известны, другая часть – новые технологии, такие, как пептидная или нуклеинокислотная. Наиболее известные технологии имеют в своей основе живой вирус, который не может вызвать заболевания. Например, эта технология используется при производстве вакцин, которые защищают от краснухи, оспы. Инактивированный, мёртвый вирус, вызывающий сильную реакцию антител, широко применяется в производстве вакцин против гриппа. На стадии разработки в настоящее время находится целый ряд различных технологий создания вакцин, потому что неизвестно, которые из них успешно подтвердят эффективность и безопасность в рамках клинических испытаний. Также отдельные вакцины могут быть непригодными для определённых групп жителей, например, для пациентов с нарушениями иммунитета или пожилых людей.
Дополнительная информация о процедуре ускоренной регистрации, или утверждении, лекарственных средств
- Ускоренная оценка – это один из инструментов Европейского Агентства по лекарственным средствам, который определён нормативными актами, чтобы ускорить оценку многообещающих лекарственных средств, в том числе и вакцин, в чрезвычайных ситуациях здоровья общества.
- В обычных условиях все данные об эффективности, безопасности и качестве лекарственных средств, а также все необходимые для регистрации лекарственного средства документы желающее зарегистрировать лекарство предприятие должно подавать в виде официальной заявки перед началом оценки.
- В случае ускоренной оценки (rolling review) Европейское Агентство по лекарственным средствам оценивает данные ещё только проходящих в это время испытаний, как только эти данные становятся доступными (производитель из представляет для оценки), и принимает решение, в какой момент эти данные станут достаточными, чтобы предприятие могло представить официальную заявку на регистрацию лекарственного средства. Оценивая данные по мере того, как они становятся доступны, Европейское Агентство по лекарственным средствам может быстрее принять решение о том, можно ли произвести регистрацию соответствующего лекарственного средства.
- Это означает, что ускоренная процедура регистрации может быть завершена в течение примерно 70 дней, по сравнению с обычной практикой осуществления регистрации, которая проходит в течение 210 дней.
- Требования к регистрации ни в какой мере не облегчаются для вакцин против Covid-19. В основе экономии времени лежит оценка доказательств – как только испытания завершаются, они незамедлительно передаются для проверки в Европейское Агентство по лекарственным средствам.
- Также следует указать, что Европейское Агентство по лекарственным средствам также уже предоставила фармацевтическим предприятиям несколько десятков научных рекомендаций (консультаций), касающихся разработки вакцин, с тем чтобы помочь разработать более приемлемый план клинических испытаний лекарственных средств.

- К настоящему моменту в Европейское Агентство по лекарственным средствам поданы четыре заявки на утверждение вакцин против Covid-19 в Европейском Союзе.
1) 21 декабря 2020 года Европейское Агентство по лекарственным средствам рекомендовало зарегистрировать с условиями вакцину "Comirnaty", которую разработали компании BioNTech и Pfizer, в тот же самый день её утвердила и Европейская Комиссия для применения на всей территории Европейского Союза. Вакцина против Covid-19 предусмотрена для применения жителям старше 5 лет. Больше информации по рекомендации зарегистрировать эту вакцину доступно здесь.
2) 6 января 2021 года Европейское Агентство по лекарственным средствам рекомендовало зарегистрировать с условиями вакцину, которую разработала компания Moderna ("Spikevax"), в тот же самый день её также утвердила и Европейская Комиссия для применения на всей территории Европейского Союза. Вакцина против Covid-19 предусмотрена для применения жителям старше 6 лет. С более подробной информацией можно ознакомиться здесь.
3) 29 января 2021 года Европейское агентство лекарств рекомендовало в Европейском союзе (ЕС) зарегистрировать на условиях вакцину “Vaxzevria”. Эта вакцина предназначена для предотвращения болезни Covid-19 для людей с 18 лет. С более подробной информацией можно ознакомиться здесь.
4) 11 марта 2021 года Европейское агентство лекарств рекомендовало в Европейском союзе (ЕС) зарегистрировать с условиями вакцину Janssen Covid-19. Эта вакцина предназначена для предотвращения инфекции коронвируса для людей с 18 лет.
5) 20 ноябрь 2021 года Европейское агентство лекарств рекомендовало в Европейском союзе (ЕС) зарегистрировать с условиями вакцину «Nuvaxovid» (предприятия "Novavax").
6) 23 июня 2022 года Европейское агентство лекарств рекомендовало в Европейском союзе (ЕС) зарегистрировать Valneva вакцину “COVID-19 Vaccine (inactivated, adjuvanted) Valneva”.
7) В настоящее время в процессe ускоренной регистрации Европейское агентство лекарств (EZA) оценивает заявление "Sputnik V", "Sinovac", "Vidprevtyn (Sanofi Pasteur) и "Covid-19 Vaccine HIPRA" (HIPRA Human Health S.L.U.).
- В настоящее врем продолжается разработка вакцин. Европейское Агентство по лекарственным средствам будет подвергать тщательной научной оценке предоставляемые данные о безопасности, эффективности и качестве каждой вакцины, точно так же, как в случае с любым представленным на утверждение лекарственным средством.
- Европейское Агентство по лекарственным средствам после тщательной оценки констатирует, что представленные научные доказательства свидетельствуют, что вакцина против Covid-19 является эффективной, качественной и безопасной, а именно – что положительное приобретение, которое может предоставить эта вакцина, превышает возможные риски, Европейское Агентство по лекарственным средствам эту вакцину, так же как и любую другую вакцину, по возможности в наикратчайшее время утвердит (зарегистрирует) для использования во всём Европейском Союзе.
- Как уже сказано, Европейское Агентство по лекарственным средствам проводит оценку вакцин против Covid-19 согласно таким же самым стандартам качества, безопасности и эффективности, как и для других лекарств, ибо не делается никаких отступлений от этих основных требований. Несмотря на то, что пока невозможно предугадать точную общую продолжительность процесса оценки, благодаря экономии времени, которую предоставляет ускоренная оценка, всё же будет сохранена строгая доказательная база на равноценном уровне, соответствующем ситуации до эпидемии.
- Всего клинические испытания в настоящий момент проходят ещё несколько десятков потенциальных вакцин против Covid-19, и в испытания вакцины от каждого производителя вовлечено несколько десятков тысяч человек. Информация обо всех клинических испытаниях доступна в Европейском регистре клинических испытаний.
- Одновременно прилагаются все усилия, чтобы и после регистрации вакцины её эффективность и безопасность находилась бы под тщательным надзором и велось обобщение и анализ всех данных.
Какие и сколько данных необходимо, чтобы утвердить надёжную и эффективную вакцину?
- Разработчики вакцины против Covid-19 в Европейское Агентство по лекарственным средствам должны подать определённые данные, по которым проводится углублённая оценка. Опираясь на результат оценки, Европейское Агентство по лекарственным средствам представляет научное заключение о безопасности, эффективности и качестве вакцины, а также о том, насколько она приемлема для вакцинирования пациентов.
- Данные должны показывать эффективность вакцины, а именно, как в клинических условиях она может предохранять человека от вызываемого вирусом Covid-19 заболевания различной степени тяжести, а также демонстрировать безопасность вакцины.
Дополнительная информация
Эффективность определяется путём оценки того, насколько эффективно вакцина предохраняет от заболевания, которое проявляется в виде определённых симптомов. Covid-19 является новым инфекционным заболеванием, и для неё неизвестны какие-либо другие показатели, например, количество антител в крови, которые можно было бы использовать, чтобы определить, насколько эффективно вакцина предохраняет от заболевания. Требования к безопасности вакцины против Covid-19 точно такие же, как в отношении любой другой вакцины в Европейском Союзе. Они не будут снижены в условиях эпидемии.
Сколько времени действует обеспечиваемая вакциной защита?
- Вирус SARS CoV-2 новый, также мало данных и об иммунитете, который возникает в результате инфицирования им. Также в настоящий момент недостаточно знаний о том, сколько времени будет действовать иммунитет, обеспечиваемый вакциной, и будет ли необходимость в периодическом получении дополнительных доз вакцины для обеспечения устойчивой продолжительной защиты.
- Данные долгосрочных исследований иммуногенетики и эффективности вакцины предоставят и информацию, которая позволит принимать в решения в отношении дальнейших планов вакцинации.
Сможет ли вакцина защитить пациентов, если вирус мутирует?
- Вирусы меняются и приспосабливаются к воздействиям факторов окружающей среды – мутируют. А именно меняется генетический материал их строения. Мутации могут происходить на различных степенях развития вирусов, и обычно они не влияют на качество действия вакцины. Некоторые вакцины эффективны в борьбе с вирусами на протяжении десятилетий после их разработки и обеспечивают долгосрочную защиту, например, вакцины против кори, краснухи, полиомиелита. В свою очередь вирусная основа таких инфекций, как, например, грипп, меняется так часто и в такой степени, что каждый год вакцину приходится приспосабливать к новым циркулирующим основам вируса и приходится вакцинироваться заново, чтобы обеспечить защиту против новых основ и типов вируса.
- Как связанные с вакцинами против Covid-19 учёные, так и ответственные регулирующие инстанции также и в дальнейшем будут отслеживать и оценивать, не меняется ли коронавирус SARS-CoV 2 с течением времени и, если меняется, насколько вакцина защищает человека от новых видов этого вируса.
Как осуществляется надзор за безопасностью и эффективностью вакцины после её утверждения с целью получения информации об эффективности вакцины в реальной жизни?
- Так же как и все лекарственные средства, вакцины тоже имеют пользу и риски, и нет таких вакцин, которые всегда были бы эффективными в 100 % случаев при всех условиях жизни.
- Государственное агентство по лекарственным средствам после утверждения вакцин против Covid-19 будет непрерывно следить за данными о безопасности и эффективности вакцин, в том числе будет обобщать и анализировать сведения о нежелательных событиях после вакцинации.
Как будет обеспечена доступность вакцины для жителей Латвии?
Следует учитывать, что регистрация лекарственного средства и его закупка – это два независимых процесса. Все новые биологические лекарственные средства, в том числе вакцины, в Европейском Союзе регистрирует Европейское Агентство по лекарственным средствам, и их регистрация становится действительной сразу во всём Европейском Союзе. В свою очередь, закупки вакцин против Covid-19 для стран-участниц координирует Европейская Комиссия, а в Латвии ответственным за закупки учреждением является Национальная служба здоровья. Однако в то время, пока вакцины ещё только проходили процесс регистрации, шла подготовка к их закупке, чтобы из-за закупочных процедур не произошло бы задержки с поставками и чтобы вакцины были доступны одновременно в одинаковых объёмах во всех странах-участницах ЕС. Больше информации о вакцинировании и о Стратегии вакцинирования против Covid-19 – здесь и в новости на интернет-странице Министерства здравоохранения от 17 ноября 2020 года.
Где будет доступна дополнительная информация?
- Мы призываем использовать только официальные и опирающиеся на доказательства источники информации о разработке вакцин против Covid-19, например, раздел «новости о Covid-19» на интернет-странице Государственного Агентства по лекарственным средствам, интернет-страницу Европейского Агентства по лекарственным средствам, где размещаемая информация регулярно дополняется.
- Государственное агентство по лекарственным средствам будет предоставлять специалистам здравоохранения и жителям в Латвии дополнительную информацию на латышском и русском языках своевременно, сразу как она будет доступна.
Дополнительная информация: почему необходимы вакцины?
- Вакцины защищают человека от серьёзных и опасных для жизни инфекционных заболеваний. Например, от гриппа, дифтерии, столбняка, коклюша, менингококковой инфекции, инвазивной пневмококковой инфекции и полиомиелита.
- Каждый год вакцинация помогает 2,7 миллионам человек во всём мире не заболеть корью, одному миллиону – не заболеть коклюшем, и двум миллионам детей – не получить столбняк.
- Несколько десятков лет назад многие люди умирали от болезней, которые теперь ликвидированы с помощью вакцинации. Люди больше страдали также и от вызванных этими болезнями осложнений, например, от слепоты, которую вызывала корь. Дети, матери которых во время беременности болели краснухой, рождались с нарушениями слуха вплоть до состояния полной глухоты, с катарактой или позже сталкивались с затруднениями в процессе обучения. Полиомиелит был главной причиной смерти, паралича и необратимой инвалидности в Европе и других регионах.
- Вакцинация помогает предупредить распространение болезни в обществе. Если большая часть жителей вакцинирована, то инфекционная болезнь не может легко распространяться. Это явление называется коллективным иммунитетом. Вакцинация может предотвратить заболевание или значительно уменьшить количество новых случаев инфицирования.
- Благодаря вакцинации, оспа теперь уничтожена во всём мире, перенос полиомиелита прекратился в большей части стран мира, в том числе в Европе.
- Вакцинация – это лучший способ, как приобрести иммунитет против болезни, по сравнению с иммунитетом, который приобретается после перенесения этого заболевания. Вакцинация не позволяет проявиться симптомам заболевания у человека, которые могу быть тяжёлыми. В отличие от других лекарственных средств, вакцины – единственные, которые не лечат болезнь, а уменьшают возможность заболеть определёнными инфекционными болезнями.
Больше информации о вакцине против Covid-19
В настоящий момент не известно, какой уровень защиты против заболевания Covid-19 будут обеспечивать вакцины, находящиеся в процессе разработки и утверждения. Эффективные вакцины вместе с другими мерами по защите общества и возможностями лечения будут являться главным фактором риска в борьбе с Covid-19.
Вакцины подготавливают иммунную систему человека (естественную защиту тела) к тому, чтобы она могла опознать и защитить организм от специфического заболевания. Большая часть вакцин-кандидатов против Covid-19 в качестве главной цели опознания вируса SARS CoV-2 используют характерный для этого вируса поверхностный белок (называемый Спайк-протеин). Когда человек получает вакцину, иммунная система обучается узнавать эти особые элементы поверхности вируса (например, Спайк-протеин). Если в организм человека попадает вирус, против которого получена вакцина, клетки иммунной системы их опознают и различными путями не позволяют ему вызвать заболевание. А именно: если человек вакцинирован и позднее инфицировался вирусом, иммунная система опознаёт этот вирус, потому что она уже подготовлена к нападению на вирус, и защищает организм от Covid-19.
Часто задаваемые вопросы пациентов
Можно ли аллергичным людям (с аллергией на укусы пчел, продукты питания и пр.) вакцинироваться против Covid-19?
Лицам, которые страдают от аллергии на любую из составных частей вакцины или от тяжёлой аллергии после получения первой дозы, необходимость вводить вторую дозу нужно обсудить со специалистом. Аллергия на любой продукт питания или укусы пчёл, ос и прочих насекомых не является противопоказанием к вакцинации.
Как скоро после переносённого Covid-19 можно вакцинироваться?
Вакцинироваться можно и сразу после переносённого заболевания, но, чтобы эффективно использовать ограниченное количество вакцин, советуем это отложить на три месяца после выздоровления от Covid-19. Согласно результатам последних научных исследований примерно 90 дней после переносённого заболевания являются периодом, после которого повторная инфекция маловерoятна.
Если человек получает первую вакцину и заболевает Covid-19, когда он может получить вторую вакцину?
Вакцинацию желательно закончить сразу после переносённого заболевания и окончания времени изоляции, если интервал уже превышает рекомендуемое время получения второй дозы. Примечание! Нет необходимости начать вакцинацию заново, вне зависимости от интервала с момента первой дозы вакцины.
Можно ли получать вакцину от Covid-19 в другое время, не в течении 21 дня?
Вторая доза вакцины должна быть получена максимально близко к 21 дню. Если из-за объективных причин невозможно получить вторую дозу сразу после 21 дня, это возможно сделать и позже.
Можно ли вакцинироваться от Covid-19 в случае, если у человека немного поднялась температура?
Небольшая простуда, насморк и. п. симптомы не являются причиной не вакцинировать пациента. Если пациент плохо себя чувствует или испытывает симптомы острой инфекции, по нынешним эпидемиологическим рекомендациям он должен оставаться дома.
Можно ли заболеть Covid-19 после получения первой дозы вакцины?
Да, такое возможно, если пациент заразился вирусом SARS-CoV-2 недолго перед или после получения вакцины. Стоит учитывать, что пациент приобретает полноценный иммунитет только после получения второй дозы. Вакцинацию желательно закончить сразу после окончания заболевания и времени изоляции.
Насколько устойчив иммунитет к Covid-19 после вакцинации?
На данный момент не хватает данных, чтобы определить продолжительность активного иммунитета.
Какая из вакцин от Covid-19 лучше?
Нет вакцины, которая была бы лучше или хуже другой. Учитывая разные принципы действия и на основании доступных данных, на данный момент не можем выделить какую-то одну вакцину из общего числа.
Какие побочные эффекты можно ожидать после вакцинации от Covid-19?
Боль в месте инъекции (>80%), усталость (>60%), головная боль (>50%), миалгия и озноб (>30%), артралгия (>20%), лихорадка и отёк в месте инъекции (>10%).
Где и когда вакцину от Covid-19 сможет получить человек, который не входит в приоритетную группу?
Каждая группа людей в порядке приоритета получит информацию по различным каналам, в том числе через СМИ, общественные организации, электронные каналы. Также информация будет передана семейным врачам. Пациенты смогут получить вакцину в больницах, поликлиниках, а также у некоторых семейных врачей. После получения информации про начало вакцинации лиц Вашей приоритетной группы, просим Вас связаться с ближайшим медицинским учреждением, которое проводит вакцинацию. Информация про кабинеты вакцинациии, где можно будет получить вакицину от Covid-19, будет доступна на домашних страницах Центра по контролю и профилактике заболеваний (SPKC) и Государственного агенства лекарств (ZVA).
- Видео о вакцинах: 11 декабря 2020 года, пресс-конференция Министерства здравоохранения: ассоциированный профессор Даце Завадска, председатель Государственного совета по иммунизации, инфектолог, глава Центра семейной вакцинации Детской клинической университетской больницы
- Последние новости об оценке эффективности вакцин:опубликованы в разделе домашней страницы > “Covid-19 ziņas”)
- Часто задаваемые вопросы о вакцинах против Covid-19













